Inhaltsverzeichnis
Die Frage, warum Zellen altern und wie dieser Prozess auf molekularer Ebene gesteuert wird, beschäftigt die biomedizinische Forschung seit Jahrzehnten. Im Zentrum dieser Überlegungen stehen die Telomere – spezialisierte Strukturelemente an den Enden der Chromosomen, die sich zunehmend als Schlüsselfaktoren in der Regulation von Zelllebensdauer und Gewebshomöostase erweisen. Ihre Verkürzung im Verlauf wiederholter Zellteilungen gilt heute als einer der zentralen Mechanismen der zellulären Seneszenz und des organismischen Alterns. Gleichzeitig eröffnen Erkenntnisse zur Telomerbiologie neue Ansätze in der Altersmedizin und regenerativen Therapie. Welche Funktion Telomere genau übernehmen, welche Rolle sie beim Altern spielen und mit welchen Erkrankungen sie assoziiert sind, beleuchtet dieser Artikel.
Inhaltsverzeichnis
Telomere – Definition
Telomere sind repetitive DNA-Sequenzen, die bei Menschen typischerweise aus Tausenden Wiederholungen der Sequenz TTAGGG bestehen. Diese Endabschnitte der Chromosomen werden von einem Proteinkomplex, dem sogenannten Shelterin-Komplex, stabilisiert und vor enzymatischem Abbau oder irrtümlicher Reparatur durch zelluläre DNA-Reparaturmechanismen geschützt. Ihre Hauptfunktion besteht darin, die Integrität des Genoms bei jeder Zellteilung zu bewahren.
Telomere – Funktion
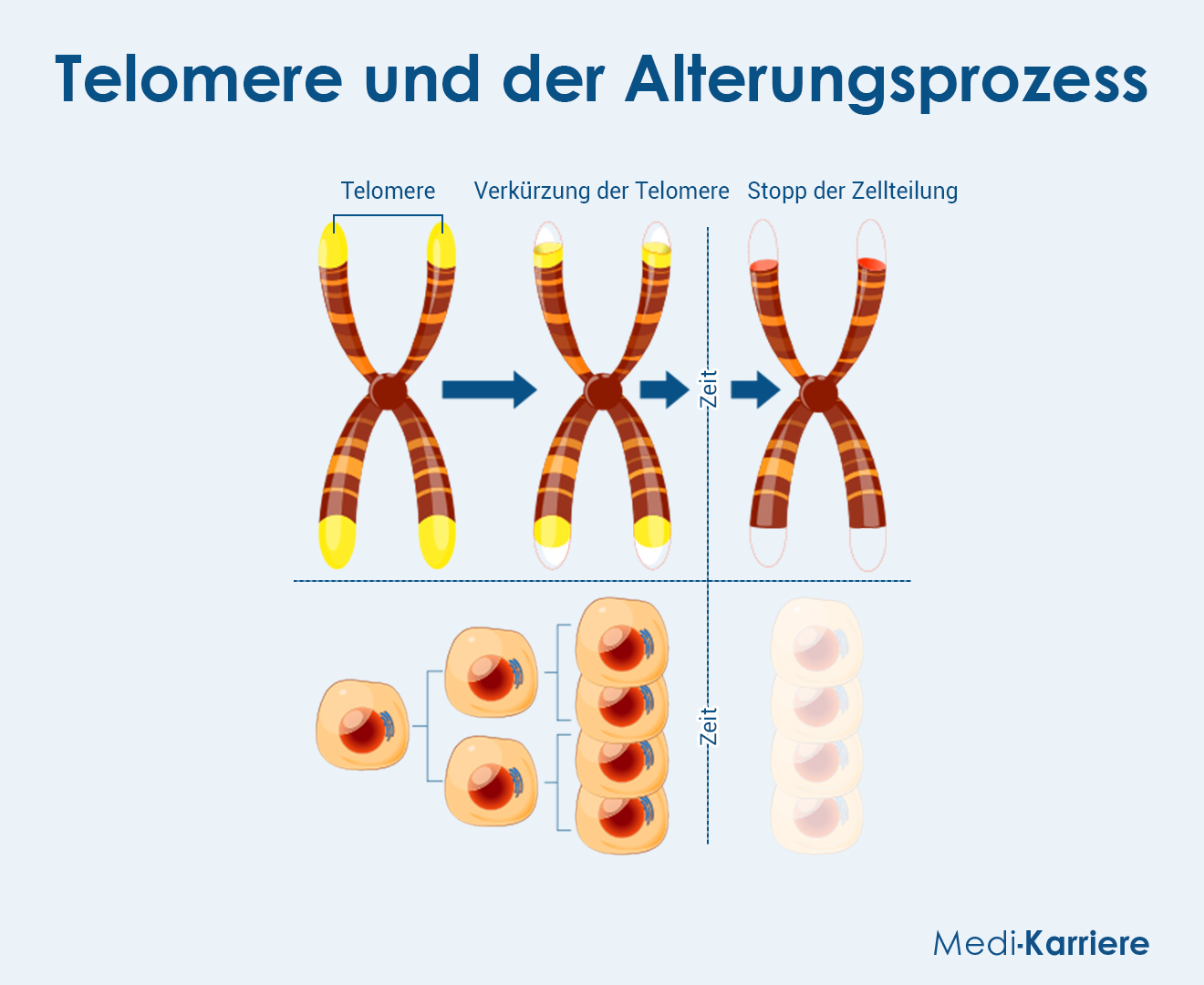
Die essentielle Aufgabe der Telomere liegt im Schutz des Erbguts vor dem Verlust wichtiger genetischer Information während der Zellteilung. Aufgrund des End-Replikationsproblems, welches den Umstand, dass die DNA-Polymerase den 3’-Endbereich der linearen DNA-Stränge nicht vollständig replizieren kann, beschreibt, verlieren Zellen mit jeder Teilung ein Stück Telomer-DNA. Sobald eine kritische Verkürzung erreicht ist, wird der Zellzyklus durch spezifische Kontrollmechanismen (zum Beispiel Aktivierung von p53) dauerhaft gestoppt. Der Zellzustand, der daraus resultiert, ist die replikative Seneszenz, ein irreversibler Wachstumsarrest, der als Schutzmechanismus vor malignem Zellverhalten dient.
Telomere – Bedeutung fürs Altern
Telomere gelten als molekularer Indikator für das biologische Alter einer Zelle. Mit jeder Zellteilung wird die Telomerreserve kleiner. Dies ist ein Prozess, der insbesondere in Geweben mit hoher Regenerationsrate (zum Beispiel Epithelien, hämatopoetisches System) zur funktionellen Erschöpfung führen kann. Gleichzeitig sind verkürzte Telomere mit der Akkumulation seneszenter Zellen verbunden, die entzündungsfördernde Botenstoffe (SASP, steht für senescence-associated secretory phenotype) freisetzen und so chronisch-entzündliche Milieus fördern. Dieser Prozess trägt wesentlich zur Entwicklung altersassoziierter Erkrankungen wie Atherosklerose, Osteoporose, Typ-2-Diabetes und Demenz bei.
Telomerase
Das Enzym Telomerase ist in der Lage, Telomere aktiv zu verlängern, indem es neue TTAGGG-Sequenzen an die Chromosomenenden anfügt. Es besteht aus einer katalytischen Untereinheit (hTERT) und einer RNA-Komponente (hTR oder TERC), die als Matrize für die DNA-Synthese dient. Während die Telomerase in den meisten somatischen Zellen abgeschaltet ist, bleibt sie in Stammzellen, Keimbahnzellen und in vielen Tumorzellen aktiv. In malignen Zellen führt die Reaktivierung der Telomerase zur Umgehung der replikativen Seneszenz und zur potenziell unbegrenzten Teilungsfähigkeit. Dies ist ein zentraler Mechanismus der Tumorentstehung.
Die Aktivität der Telomerase wird durch zahlreiche regulatorische Faktoren beeinflusst, darunter epigenetische Modifikationen, Transkriptionsfaktoren (zum Beispiel c-Myc) sowie inflammatorische und hormonelle Signalwege.
Einfluss von Umweltfaktoren und Lebensstil
Interessanterweise unterliegt die Telomerlänge nicht nur genetischer Kontrolle, sondern wird auch durch äußere Einflüsse moduliert. Studien zeigen, dass chronischer psychosozialer Stress, oxidativer Stress, Rauchen, Fettleibigkeit und körperliche Inaktivität mit einer beschleunigten Telomerverkürzung assoziiert sind. Umgekehrt konnten Meditation, körperliche Aktivität, eine antioxidative Ernährung sowie ein stabiles soziales Umfeld mit einer verlangsamten Telomererosion oder sogar einer teilweisen Verlängerung assoziiert werden. Diese Beobachtungen lassen vermuten, dass die Telomerbiologie eine Schnittstelle zwischen Umwelt, Verhalten und Zellgesundheit darstellt.
Evolutionäre Perspektiven
Aus evolutionsbiologischer Sicht stellt die Telomerverkürzung einen Mechanismus dar, der die Anzahl möglicher Zellteilungen begrenzt. Dies hat das Ziel, die Entstehung von Krebszellen durch unkontrolliertes Wachstum zu verhindern. Der Preis dieses Schutzmechanismus ist jedoch die eingeschränkte Regenerationsfähigkeit im höheren Lebensalter.
Unterschiede bei verschiedenen Tierarten
Interessanterweise zeigen verschiedene Tierarten große Unterschiede in Telomerstruktur, -länge und -regulation, was Rückschlüsse auf ihre Lebenserwartung, Krebsanfälligkeit und Reproduktionsstrategien zulässt. Arten wie Nagetiere besitzen kurze Telomere mit wenig Telomeraseaktivität, während langlebige Arten wie manche Vögel oder Wale lange Telomere und stabile Telomeraseexpression aufweisen. Hieraus ergibt sich ein Hinweis auf artspezifische evolutionäre Kompromisse zwischen Langlebigkeit und Tumorsuppression.
Telomere – Erkrankungen
Mutationen in Genen der Telomerase oder anderer telomerassoziierter Proteine können zu einer Gruppe seltener genetischer Erkrankungen führen, die unter dem Begriff Telomeropathien oder telomerassoziierte Syndrome zusammengefasst werden. Zu den bekanntesten zählen:
- Dyskeratosis congenita
- Idiopathische Lungenfibrose
- Aplastische Anämie
- Leberzirrhose im Kindesalter
Gemeinsam ist diesen Erkrankungen eine beschleunigte Telomerverkürzung und eine frühe Erschöpfung regenerativer Zellreserven. Die klinische Manifestation ist vielfältig, betrifft jedoch häufig blutbildende, epitheliale und pulmonale Gewebe.
- Replikation und Reparaturmechanismen der DNA, https://next.amboss.com/... (Abrufdatum: 07.04.2025)